陜西專業臨床前動物實驗哪家好
臨床前動物實驗,TGN1412是TeGenero的較早產品,從生產到進入臨床試驗才2年多時間,從MHRA批準TGN1412進入臨床試驗到試驗開始總共才45天。ESG指出,雖然臨床前動物實驗沒有發現嚴重不良反應,但不能因此估測出一個TGN1412用于人類的安全劑量,藥物的安全性未得到充分論證。實施臨床試驗的研究者沒有受到良好培訓,志愿者對可能發生的危險也了解不足。媒體和公眾都指責MHRA為了吸引醫藥公司到英國進行臨床研究而放寬了藥物臨床研究的審批。從而使一家*有15名雇員、風險資本驅動的德國小公司不在本國進行臨床試驗,卻轉而選擇英國。化學藥臨床前動物實驗是什么?陜西專業臨床前動物實驗哪家好
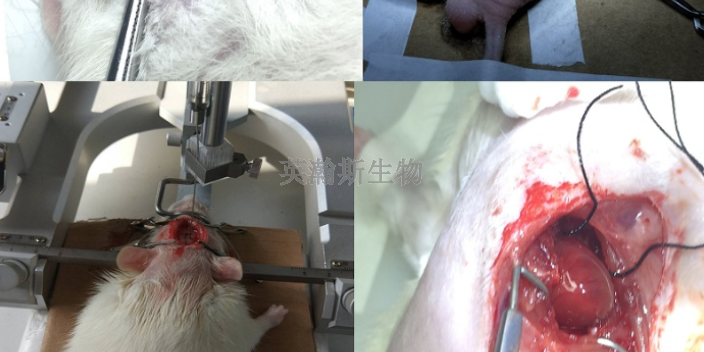
關于臨床前動物實驗的故事。過去十余年,國內某團隊也一直致力于理想的“超級疫苗”研究,基于已有的研究基礎,在此次**科研攻關中,他們設計出新的疫苗抗原分子,建立哺乳動物細胞表達系并純化了抗原蛋白,用微劑量免疫動物后(小動物5微克,大動物10微克),產生了高達百萬倍試紙測試效價的抗體。免疫抗體經在國家批準的P3實驗室測定,中和病毒的效價都達到了要求,有的超過了檢測單位設定的比較高限。目前,他們已開始進行臨床前動物實驗,在免疫猴子、小鼠和雪貂準備攻毒中和實驗。江蘇專注臨床前動物實驗檢測生物藥臨床前動物實驗研究;
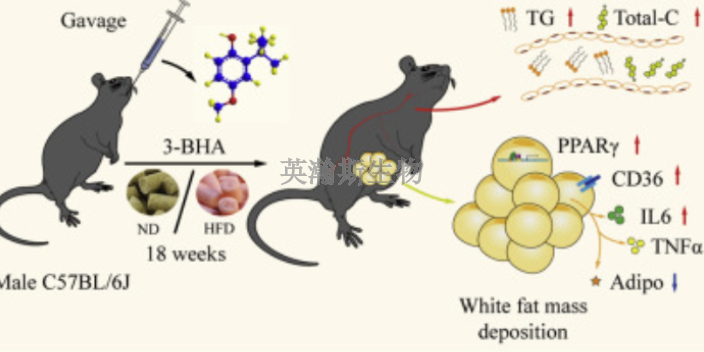
從臨床前動物實驗到臨床試驗,路在何方?這樣的悲劇也揭示了一個令人不安的事實,人們對人類免疫系統的認識還存在很多盲點,而動物實驗和臨床試驗也經常出現相左的結果。那么,我們現有的臨床試驗體系是否安全可靠?為了防止這樣的悲劇再次發生,應該如何設計臨床試驗?從動物實驗到人體試驗,路該如何走?ESG根據調查結果并普遍征詢了**意見后提出22條關于如何改善初次用于人體藥物的Ⅰ期臨床試驗安全性建議。主要關注如何計算初次應用的藥物劑量、如何給藥;不同研究組織和醫藥公司應共享有關藥物臨床試驗不良反應(特別是未發表的)、失敗的藥物試驗等資料;特殊藥物,例如作用于人體生理過程的生物藥物,在進行研究之前應征求單獨**的意見等。
臨床前動物實驗模型選擇的思路應遵循以下原則:一是要很大程度地模擬預期臨床應用的實驗系統,包括動物及其相關環境和生理特性。二是臨床前動物實驗研究實施的合理性,風險分析要素應涉及為什么選擇該動物模型。如果動物模型有局限性,器械的一些相關風險比較好通過實驗室或者尸體實驗進行評價,并確定其相關性。除此之外,還應確定實驗系統的遺傳學差異(動物和人的差異)。如實驗系統和人的不同、器械的尺寸和輸送系統差異、器械植入的部位和追蹤方式差異,等等。化學藥臨床前動物實驗外包;

臨床前動物實驗除了《藥物非臨床研究質量管理規范》第十八條對受試物和對照品的使用和管理的基本要求之外,鑒于醫療器械的受試物多為固體材料或器械,建議普遍表征研究中使用的所有受試物和對照品。由于不斷的工藝改進和優化,委托方可能在開始臨床研究之前研發多次重復的受試物,因此建議在關鍵的臨床前動物實驗研究使用**比較終臨床設計的受試物。如果沒有使用比較終設計的受試物,應確定比較終的臨床設計樣品與動物實驗研究的設計相比,對患者沒有新的風險。建議將受試物和對照品包裝、消毒,并以與臨床產品相同的方式運送到研究現場。應開發一種從采購到使用過程中全程追蹤試驗器械和對照器械的方法。英瀚斯專業做醫療器械臨床前動物實驗外包。重慶有什么臨床前動物實驗機構
化妝品臨床前動物實驗包括哪些?陜西專業臨床前動物實驗哪家好
臨床前動物實驗到Ⅰ期臨床試驗——安全之路?——TGN1412Ⅰ期臨床試驗的慘痛教訓的相關知識。2007年1月27日,來自英國倫敦帝國學院、倫敦國王學院和Babraham研究所的學者報告,人體的記憶T細胞可能是2006年3月造成抗CD28人源化單克隆抗體(TGN1412)Ⅰ期臨床試驗悲劇的原因。抗CD28人源化單克隆抗體——TGN1412Ⅰ期臨床試驗災難性意外是2006年醫藥行業的熱點新聞。對此,英國成立的單獨**小組(ESG)曾召開過10多次會議,并于2006年12月7日發布了比較終研究報告。英國藥物和保健品管理局(MHRA)也將于2007年2月6日召開研討會以探討從TGN1412事件中吸取的教訓。對這一事件的回顧與分析無疑有助于人們更深入的思考藥物試驗面臨的一些問題。陜西專業臨床前動物實驗哪家好
- 浙江腦缺血再灌注模型多少錢 2025-01-22
- 廣東MCO腦缺血再灌注模型制作 2025-01-22
- 遼寧推薦的腦缺血再灌注模型價格 2025-01-22
- 西藏哪家做腦缺血再灌注模型公司 2025-01-21
- 遼寧專門做腦缺血再灌注模型制作 2025-01-21
- 云南專門做腦缺血再灌注模型多少錢 2025-01-21
- 山東比較好的腦缺血再灌注模型實驗 2025-01-20
- 內蒙古專門做腦缺血再灌注模型 2025-01-20
- 福建腦缺血再灌注模型價格 2025-01-20
- 遼寧比較好的腦缺血再灌注模型檢測 2025-01-19
- 麗水代理奧托博克假肢公司 2025-01-22
- 陜西無菌海藻糖現貨供應 2025-01-22
- 廣東糞菌群移植廠家直銷 2025-01-22
- 南京搖床搖瓶直銷價 2025-01-22
- 綜合ELISA試劑盒 2025-01-22
- 陜西齒科氧化鋅口腔耗材精選廠家 2025-01-22
- 矯形助行器 2025-01-22
- 河南快速牙托粉顏色 2025-01-22
- 廣州遠紅外小兒***貼貼牌現貨直發 2025-01-22
- 廣西濟南脂質體載藥 2025-01-22