海南高質(zhì)量臨床前動物實(shí)驗(yàn)價(jià)格
關(guān)于臨床前動物實(shí)驗(yàn),資料顯示,截至2012年7月,衛(wèi)生部干細(xì)胞整頓工作辦公室的調(diào)查結(jié)果是——干細(xì)胞***已經(jīng)在我國300家左右的醫(yī)院、機(jī)構(gòu)開展。而國家干細(xì)胞工程技術(shù)研究中心主任、中國醫(yī)學(xué)科學(xué)院血液學(xué)研究所研究員韓忠朝認(rèn)為,300家醫(yī)療機(jī)構(gòu)是個保守的數(shù)字,“這是衛(wèi)生部開展的一個自查,自己報(bào)上的有300家,還有沒有報(bào)上去的呢?實(shí)際肯定不止300家做”。事實(shí)上,除了造血干細(xì)胞***血液疾病以外,衛(wèi)生部沒有批準(zhǔn)任何一家醫(yī)療機(jī)構(gòu)用干細(xì)胞臨床***任何一種疾病,全球的絕大多數(shù)干細(xì)胞研究都在臨床前動物實(shí)驗(yàn)或臨床階段,只有加拿大在2012年5月份批準(zhǔn)了美國一家公司生產(chǎn)的干細(xì)胞藥物用于***移植物抗宿主病、日本iPS細(xì)胞實(shí)驗(yàn)自去年來得到**支持。化學(xué)藥臨床前動物實(shí)驗(yàn)研究;海南高質(zhì)量臨床前動物實(shí)驗(yàn)價(jià)格
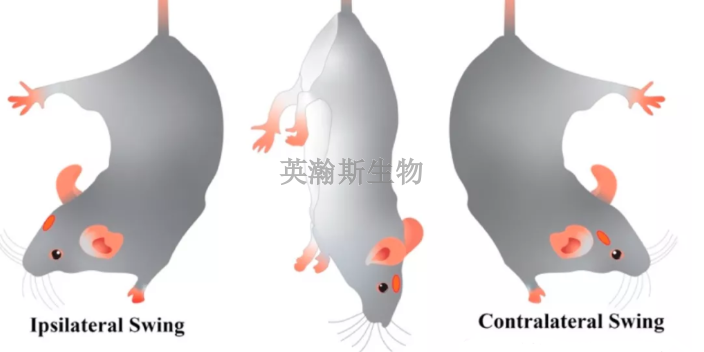
作為**個可植入的、第三代心室輔助裝置——磁液雙懸浮血泵“火箭心”,已經(jīng)進(jìn)入批量生產(chǎn)的臨床前動物實(shí)驗(yàn)期。目前進(jìn)行的動物實(shí)驗(yàn)主要是觀察血泵的血液動力學(xué)參數(shù)、生物相容性以及對動物身體的影響情況。下一步將開展生物醫(yī)學(xué)和工程學(xué)檢測。完成至少6批次的動物實(shí)驗(yàn)后,即可進(jìn)入臨床試用階段。慢性心力衰竭是心血管病中比較常見而且危害比較大的疾病之一,目前我國有1600多萬心衰患者。目前對于心衰的***,一般采取藥物***、外科手術(shù)、機(jī)械輔助循環(huán)及心臟移植。四川什么是臨床前動物實(shí)驗(yàn)機(jī)構(gòu)英瀚斯專業(yè)做醫(yī)療器械臨床前動物實(shí)驗(yàn)外包。
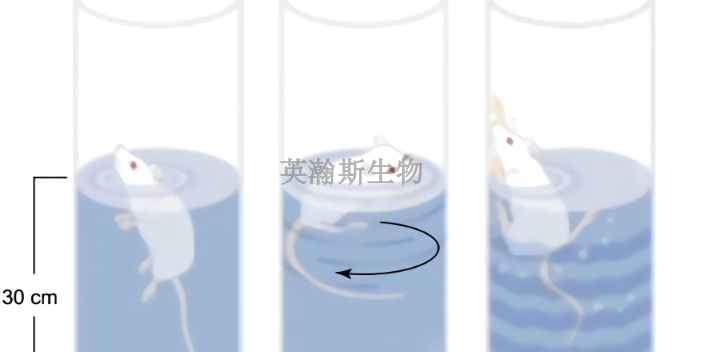
關(guān)于臨床前動物實(shí)驗(yàn)的故事。過去十余年,國內(nèi)某團(tuán)隊(duì)也一直致力于理想的“超級疫苗”研究,基于已有的研究基礎(chǔ),在此次**科研攻關(guān)中,他們設(shè)計(jì)出新的疫苗抗原分子,建立哺乳動物細(xì)胞表達(dá)系并純化了抗原蛋白,用微劑量免疫動物后(小動物5微克,大動物10微克),產(chǎn)生了高達(dá)百萬倍試紙測試效價(jià)的抗體。免疫抗體經(jīng)在國家批準(zhǔn)的P3實(shí)驗(yàn)室測定,中和病毒的效價(jià)都達(dá)到了要求,有的超過了檢測單位設(shè)定的比較高限。目前,他們已開始進(jìn)行臨床前動物實(shí)驗(yàn),在免疫猴子、小鼠和雪貂準(zhǔn)備攻毒中和實(shí)驗(yàn)。
當(dāng)臨床前動物實(shí)驗(yàn)結(jié)果顯示化合物具有足夠的安全性并準(zhǔn)備進(jìn)入人體試驗(yàn)時主辦者需要向FDA申請新藥臨床試驗(yàn)investigationalNewDrugApplication,ND申請)。按照美國食品、藥品和化妝品法案(Food,DrugandCosmeticAct),此時的化合物已經(jīng)成為研究藥物,將受到官方的監(jiān)管。FDA收到藥物申報(bào)主辦者遞交的IND時,藥物申報(bào)主辦者,即負(fù)責(zé)藥物上市的公司硏究機(jī)構(gòu)和其他組織,必須向FDA提供其對實(shí)驗(yàn)動物所進(jìn)行臨床前試驗(yàn)的結(jié)果,以及進(jìn)行人體試驗(yàn)的具體計(jì)劃。在這個階段,FDA必須判斷藥物是否安全,是否達(dá)到實(shí)施人體試驗(yàn)的標(biāo)準(zhǔn)。化藥臨床前動物實(shí)驗(yàn)包括哪些?
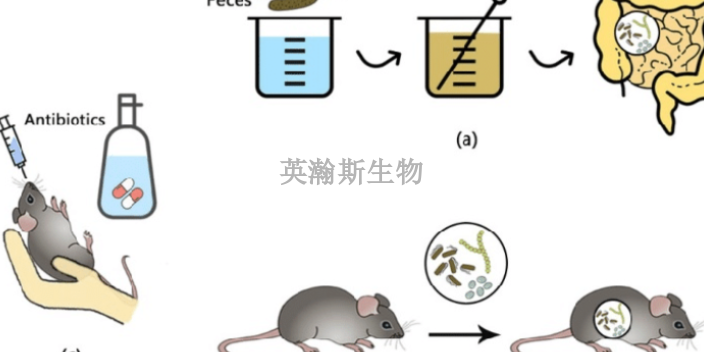
專業(yè)臨床前動物實(shí)驗(yàn)就找英瀚斯。在人類正常的科學(xué)研究歷史上,并沒有建立“人類***模型”的先例。更重要的問題是,它可能就不考慮設(shè)置對照組了。以動物疫苗的臨床試驗(yàn)舉例說,很多動物疫苗可在本種動物身上進(jìn)行臨床動物實(shí)驗(yàn),當(dāng)拿病毒去攻疫苗免疫過后的動物時,通常需要設(shè)置的是不同劑量的對照組,比較簡單的也需要設(shè)兩個組,一組是注射疫苗組,一組是注射鹽水等其他安慰劑的組,當(dāng)結(jié)果表明前者未發(fā)病,后者發(fā)病了,才能說明疫苗有效。事實(shí)上,全球?qū)τ诓《疽呙绲难邪l(fā)速度堪稱“前所未有”。生物藥臨床前動物實(shí)驗(yàn)研究;安徽專業(yè)臨床前動物實(shí)驗(yàn)指標(biāo)
英瀚斯是專業(yè)的化妝品臨床前動物實(shí)驗(yàn)外包公司。海南高質(zhì)量臨床前動物實(shí)驗(yàn)價(jià)格
醫(yī)療器械臨床試驗(yàn)前動物試驗(yàn)研究,作為在臨床試驗(yàn)之前初步驗(yàn)證醫(yī)療器械安全性及有效性的手段,對于尚沒有大量臨床應(yīng)用歷史的高風(fēng)險(xiǎn)醫(yī)療器械以及創(chuàng)新型醫(yī)療器械來說是必要的試驗(yàn)。我國在2016年3月23日發(fā)布了《醫(yī)療器械臨床試驗(yàn)質(zhì)量管理規(guī)范》,在該管理規(guī)范中,明確要求在臨床試驗(yàn)研究之前申請者應(yīng)當(dāng)完成必要的動物試驗(yàn)研究以及風(fēng)險(xiǎn)分析。關(guān)于是否需要做臨床前動物試驗(yàn)研究應(yīng)根據(jù)產(chǎn)品的風(fēng)險(xiǎn)分析進(jìn)行判斷。2019年4月19日,國家藥品監(jiān)督管理局(NMPA)發(fā)布了《醫(yī)療器械動物實(shí)驗(yàn)研究技術(shù)審查指導(dǎo)原則***部分:決策原則》,對如何決策是否有必要進(jìn)行臨床前動物實(shí)驗(yàn)研究給出了指導(dǎo)性建議。海南高質(zhì)量臨床前動物實(shí)驗(yàn)價(jià)格
- 山東真實(shí)細(xì)胞實(shí)驗(yàn)外包公司 2024-12-23
- 甘肅細(xì)胞實(shí)驗(yàn)外包檢測 2024-12-23
- 廣東醫(yī)學(xué)細(xì)胞實(shí)驗(yàn)外包推薦 2024-12-23
- 湖北專門做細(xì)胞實(shí)驗(yàn)外包哪家靠譜 2024-12-22
- 甘肅專業(yè)的細(xì)胞實(shí)驗(yàn)外包推薦 2024-12-22
- 四川靠譜的細(xì)胞實(shí)驗(yàn)外包推薦 2024-12-22
- 福建整體細(xì)胞實(shí)驗(yàn)外包 2024-12-21
- 黑龍江真實(shí)細(xì)胞實(shí)驗(yàn)外包檢測 2024-12-21
- 江蘇哪家做細(xì)胞實(shí)驗(yàn)外包 2024-12-21
- 遼寧整體細(xì)胞實(shí)驗(yàn)外包檢測 2024-12-20
- 深圳備孕凝膠多少錢 2024-12-23
- 河北莫諾苯宗供應(yīng)商 2024-12-23
- 海洋生物外泌體蛋白質(zhì)組學(xué) 2024-12-23
- 溫州轉(zhuǎn)印膜工廠 2024-12-23
- 北京抑菌乳液公司 2024-12-23
- 福建熱凝牙托粉電話 2024-12-23
- 江蘇推薦創(chuàng)面敷料哪里有賣的 2024-12-23
- iPSC培養(yǎng)生物反應(yīng)器材質(zhì)安全性數(shù)據(jù) 2024-12-23
- 河南比較好的醫(yī)用刻錄機(jī)廠家批發(fā)價(jià) 2024-12-23
- 西藏5混1病毒采樣管出口企業(yè) 2024-12-23