湖北有什么臨床前動物實驗是什么
關于臨床前動物實驗動物的選擇,假如使用非人類的靈長類動物作為研究對象,其與人類的相似度則是明顯提升了的。例如,日本科學家培育成功的南美絨猴就克服了小鼠的不足,代謝類型、生理病理以及基因組,甚至細胞相似性非常接近人類了。即便如此,其他靈長類動物實驗依然無法替代人體試驗。有資料顯示,由于對臨床前動物實驗和臨床試驗的差距認識不足,曾發生過嚴重地危害受試者安全的案例。經調查發現,造成該后果的原因就在于,一直被置于無菌環境下飼養的獼猴與人體的免疫系統有差異。試想,如果直接將此動物實驗的研究結果移植到人類身上,后果將不堪設想。化學藥臨床前動物實驗公司;湖北有什么臨床前動物實驗是什么
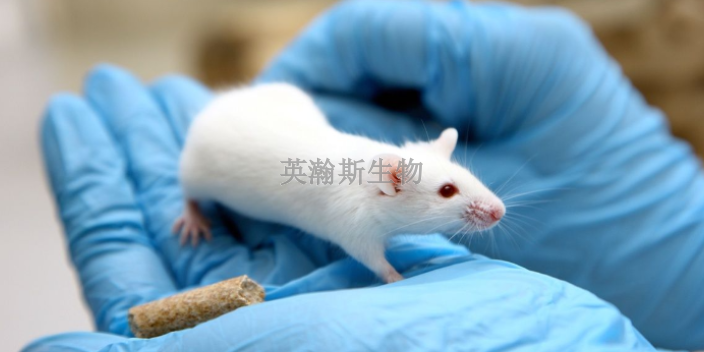
申請人應盡臨床前動物實驗的可能通過初步研究(如實驗室研究等)來驗證所確定的風險控制措施的有效性,只有在實驗室研究不足時,才能通過動物實驗進行進一步驗證。動物實驗數據可作為風險/收益分析的支持數據。1.可行性研究:可行性研究是指在產品設計和開發階段,為確認/驗證產品的工作原理、作用機理、設計、可操作性、功能性、安全性等方面,或識別新的意外風險而進行的研究。2.安全性研究:申請人采取風險控制措施后,可通過動物實驗對部分產品的安全性進行適當評價。3.有效性研究:盡管某些醫療器械在動物和人類之間的有效性可能存在一些差異,但合理設計的動物實驗可以支持產品的有效性(包括性能和操作)。河南臨床前動物實驗中藥臨床前動物實驗包括哪些?
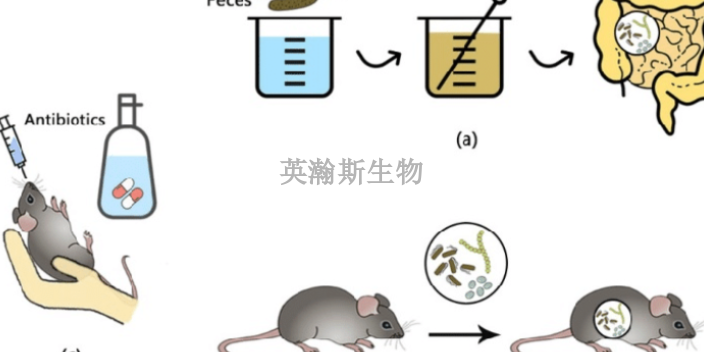
當臨床前動物實驗結果顯示化合物具有足夠的安全性并準備進入人體試驗時主辦者需要向FDA申請新藥臨床試驗investigationalNewDrugApplication,ND申請)。按照美國食品、藥品和化妝品法案(Food,DrugandCosmeticAct),此時的化合物已經成為研究藥物,將受到官方的監管。FDA收到藥物申報主辦者遞交的IND時,藥物申報主辦者,即負責藥物上市的公司硏究機構和其他組織,必須向FDA提供其對實驗動物所進行臨床前試驗的結果,以及進行人體試驗的具體計劃。在這個階段,FDA必須判斷藥物是否安全,是否達到實施人體試驗的標準。
臨床前動物實驗方案盡可能模擬臨床設計和使用。應當確認在輸送、植入或使用器械中的所有步驟,并制定每一個步驟的可接受標準。建議對每個驗收標準應用半客觀的評定量化表(例如李克特量表,Likert scale)。如果器械與輔助設備一同輸送或使用,則可接受標準應包含評估系統相容性的要素。評級標準應當囊括從器械準備到放置或使用乃至取回和重新放置過程中的所有步驟。如果器械通過手術放置,則應描述器械從進入體壁到比較終器械操作期間的所有步驟。生物藥臨床前動物實驗外包;

從臨床前動物實驗到臨床試驗,路在何方?這樣的悲劇也揭示了一個令人不安的事實,人們對人類免疫系統的認識還存在很多盲點,而動物實驗和臨床試驗也經常出現相左的結果。那么,我們現有的臨床試驗體系是否安全可靠?為了防止這樣的悲劇再次發生,應該如何設計臨床試驗?從動物實驗到人體試驗,路該如何走?ESG根據調查結果并普遍征詢了**意見后提出22條關于如何改善初次用于人體藥物的Ⅰ期臨床試驗安全性建議。主要關注如何計算初次應用的藥物劑量、如何給藥;不同研究組織和醫藥公司應共享有關藥物臨床試驗不良反應(特別是未發表的)、失敗的藥物試驗等資料;特殊藥物,例如作用于人體生理過程的生物藥物,在進行研究之前應征求單獨**的意見等。生物藥臨床前動物實驗機構;河北臨床前動物實驗指標
生物藥臨床前動物實驗研究;湖北有什么臨床前動物實驗是什么
醫療器械臨床試驗前動物試驗研究,作為在臨床試驗之前初步驗證醫療器械安全性及有效性的手段,對于尚沒有大量臨床應用歷史的高風險醫療器械以及創新型醫療器械來說是必要的試驗。我國在2016年3月23日發布了《醫療器械臨床試驗質量管理規范》,在該管理規范中,明確要求在臨床試驗研究之前申請者應當完成必要的動物試驗研究以及風險分析。關于是否需要做臨床前動物試驗研究應根據產品的風險分析進行判斷。2019年4月19日,國家藥品監督管理局(NMPA)發布了《醫療器械動物實驗研究技術審查指導原則***部分:決策原則》,對如何決策是否有必要進行臨床前動物實驗研究給出了指導性建議。湖北有什么臨床前動物實驗是什么
- 山東真實細胞實驗外包公司 2024-12-23
- 甘肅細胞實驗外包檢測 2024-12-23
- 廣東醫學細胞實驗外包推薦 2024-12-23
- 湖北專門做細胞實驗外包哪家靠譜 2024-12-22
- 甘肅專業的細胞實驗外包推薦 2024-12-22
- 四川靠譜的細胞實驗外包推薦 2024-12-22
- 福建整體細胞實驗外包 2024-12-21
- 黑龍江真實細胞實驗外包檢測 2024-12-21
- 江蘇哪家做細胞實驗外包 2024-12-21
- 遼寧整體細胞實驗外包檢測 2024-12-20
- 深圳備孕凝膠多少錢 2024-12-23
- 河北莫諾苯宗供應商 2024-12-23
- 海洋生物外泌體蛋白質組學 2024-12-23
- 溫州轉印膜工廠 2024-12-23
- 北京抑菌乳液公司 2024-12-23
- 福建熱凝牙托粉電話 2024-12-23
- 江蘇推薦創面敷料哪里有賣的 2024-12-23
- iPSC培養生物反應器材質安全性數據 2024-12-23
- 河南比較好的醫用刻錄機廠家批發價 2024-12-23
- 西藏5混1病毒采樣管出口企業 2024-12-23