江蘇大鼠實驗動物模型實驗
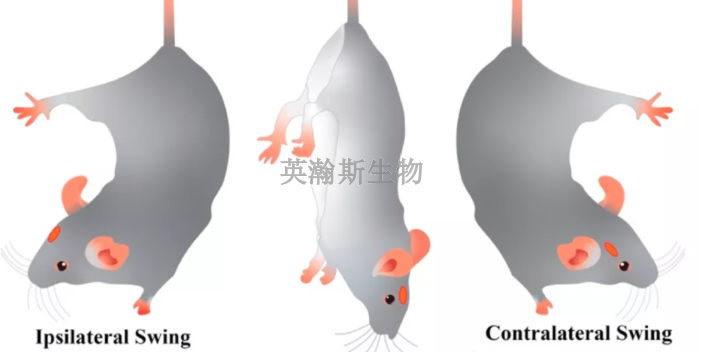
蛛網膜下腔出血系由腦底或腦表部位的血管破裂,血液破入蛛網膜下腔引起。顱內動脈瘤,腦動、靜脈畸形,血壓高動脈硬化等為常見病因。蛛網膜下腔出血后可引起腦血管痙攣。因此,蛛網膜下腔出血和遲發性腦血管痙攣的模型有許多共同之處,造模時可同時作為參考。
英瀚斯熟練掌握蛛網膜下腔出血造模,及其他動物模型。
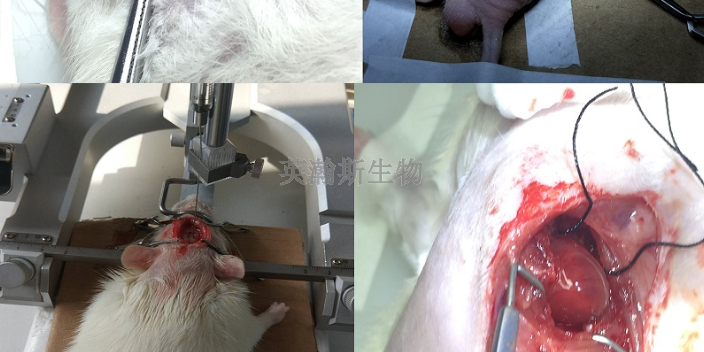
復制方法 :健康大鼠,雌雄不拘,體重為250~350g。將釣魚線剪成長約50mm,并在18mm處作標記,酒精消毒后置于無菌生理鹽水中備用。麻醉后仰臥固定,剃除頸部毛發,手術區域皮膚消毒。頸正中切口,分離右側頸總動脈、頸外動脈、頸內動脈,結扎、切斷頸外動脈分支及頸總動脈分叉處小動脈,并游離頸外動脈主干,沿著頸內動脈暴露翼腭動脈,在頸外動脈殘端放一絲線,使其呈一松結。在翼腭動脈起始部置一微動脈夾,同時夾閉頸總動脈及頸內動脈主干近端。在頸外動脈殘端剪一小口,將制備好的栓線插入。此時將頸外動脈殘端處絲線的松結拉緊,除去頸內動脈的動脈夾,繼續將絲線沿著頸內動脈插入,直至感到有阻力,這時稍用力再插入1.0~1.5mm后有落空感即可抽出絲線并除去微動脈夾。栓線的直徑及插入的深度根據動物的體重而定。 英瀚斯實驗動物模型,專業評估熟練造模,保障成功率!江蘇大鼠實驗動物模型實驗
APP 轉基因實驗動物模型,神經細胞 β-淀粉樣前體蛋白(APP)轉基因動物模型是將人源性 APP 基因與小鼠基因組整合、表達和遺傳。與正常動物相比,APP 轉基因動物腦中Aβ表達過量,引起認知功能障礙等系列AD臨床病理特征。
·PDAPP小鼠模型·轉人類APP695swe和APP717V-F基因的PDAPP小鼠模型是由C57BL/6鼠與DBA/2F1鼠雜合而生。PDAPP小鼠APP表達水平高,6~9月齡時在模型小鼠大腦多區域表現出與AD相似的病理表現,如細胞外Aβ異常沉積、突觸丟失、神經炎癥反應和小膠質細胞增生等,但NFTs形成不明顯。由于PDAPP小鼠在同月齡腦中Aβ沉積異常,主要用于與Aβ相關的AD疾病機制研究。
·Tg2576小鼠模型·Tg2576小鼠模型是轉人類APP695基因小鼠,在9~12個月時表現出學習記憶功能減退,在大腦多部位逐漸出現Aβ沉積和形成老年斑,在皮層出現星形膠質細胞聚集,該模型一般應用于早期AD的研究。 江蘇大鼠實驗動物模型實驗英瀚斯生物公司 動物房、手術操作實驗室,可制作各類實驗動物模型。

實驗動物模型建模的原則。相似性,重復性,可靠性,適用性和可控性,易行性和經濟性。在動物身上復制人類疾病模型。目的在于從中找出可以推廣(外推)應用于病人的有關規律。外推法(Extrapolation)要冒風險,因為動物與人到底不是一種生物。例如在動物身上無效的藥物不等于臨床無效,反之也然。因此,設計動物疾病模型的一個重要原則是,所復制的模型應盡可能近似于人類疾病的情況。能夠找到與人類疾病相同的動物自發性疾病當然比較好。
關于老年癡呆(阿爾茨海默癥)的實驗動物模型,英瀚斯生物小編總結。AD由于其疾病本身的復雜性,單一造模存在很大弊端,越來越多的研究趨向于復合造模,目前為止,尚無對復合造模效果的比較研究,由于AD的發病機制不夠明確,且猜想靶點和致病因素較多,世界范圍內目前未發現能夠全方面的模擬人類衰老、疾病和并發癥的動物模型。但多數學者認為,采用復合方法造模能在很大程度上表現出更為接近AD特征的模型動物,為癡呆的研究提出了更深入的探索方向。迄今為止沒有公認的AD動物模型,研究者只能從藥物和疾病本身的特征出發,選擇匹配度較高的模型用于研究。一般而言,基礎研究的藥效評價多數依賴于動物指標,所以模型的選擇、模型成功與否、能否精細造模以符合疾病特征等是實驗過程中我們需要慎重考慮的問題。而新的動物模型需要能準確地預測實驗醫療的功效,從而使藥物從實驗室到病床的轉化成為可能。實驗動物模型的造模方法?
實驗動物模型的案例。反義寡核苷酸(ASOs)是一種短的、化學合成的單鏈寡核苷酸,通過對其骨架和糖基進行修飾,可增加其穩定性、藥理特性以及與靶標的結合,并通常具有較小的毒性。常用于細胞和動物體內基因功能研究以及ASO核酸藥物的開發等。經過化學修飾的ASOs可以通過多種作用機制發揮作用。常見的一種作用方式是與RNA結合,形成RNA&DNA雜合體,依賴于RNase H發揮作用,從而導致靶標mRNA的降解,主要適用于干擾細胞核內的lncRNA/circRNA/mRNA等。小鼠實驗動物模型都有哪些?福建大鼠實驗動物模型制作
英瀚斯生物 專業承接各類實驗動物模型!江蘇大鼠實驗動物模型實驗
誘導式關節炎模型根據造模物質的不同進行分類,常見的有佐劑誘導型、膠原誘導型和膠原抗體誘導型關節炎。其中大鼠CIA模型的組織和免疫學改變與人RA**接近,AA模型的病情表現**為明顯和持續。
(一)佐劑誘導型(AA)AA,又稱為弗氏佐劑關節炎,介導溶劑分為完全佐劑(CFA)和不完全佐劑(IFA)。通常用CFA作介導劑,AA模型在T細胞相關致炎通路的藥物篩選上發揮著重要的作用。
(二)膠原誘導型(CIA)CIA模型是由Trentham等于1977年***建立的實驗性關節炎動物模型。通過皮下注射Ⅱ型膠原和等量CFA的混合液來建造,來源于雞、小牛和大鼠的Ⅱ型膠原均能引起關節炎癥。CIA是MHC相關型,以T/B淋巴細胞介導的關節炎癥侵蝕為主要特征。
(三)膠原抗體誘導型(CAIA)抗Ⅱ型膠原單克隆抗體源自8周大的雄性DBA/1J小鼠CIA模型,這些抗體混合物注射到模型小鼠的關節腔后可直接作用于Ⅱ型膠原或其他在體內高表達的自身抗原,從而發揮免疫介導作用。該模型的臨床癥狀與CIA和RA很相似,突出特點是能在幾天之內迅速發病,關節組織中巨噬細胞和多核型白細胞浸潤。該模型很好的體現了外源性抗原抗體刺激體誘導的嚴重關節損傷。 江蘇大鼠實驗動物模型實驗
- 河北專業臨床前動物實驗多少錢 2025-01-03
- 北京個性化臨床前動物實驗價格 2025-01-03
- 河南病理實驗外包實驗室 2025-01-03
- 廣西個性化臨床前動物實驗多少錢 2025-01-02
- 上海專注臨床前動物實驗研究 2025-01-02
- 黑龍江臨床前動物實驗研究 2025-01-02
- 寧夏靠譜的病理實驗外包實驗室 2025-01-01
- 河南專業臨床前動物實驗 2025-01-01
- 天津臨床前動物實驗檢測 2025-01-01
- 湖南推薦的臨床前動物實驗評價 2024-12-31
- 湖南4K手術直播會診大概多少錢 2025-01-03
- 生物樣品進口風險評估哪家好 2025-01-03
- 子午流注產品中醫產品推薦 2025-01-03
- 天津二維運動混合機結構圖 2025-01-03
- 云南效果白夫康表皮抑菌膏市場價格 2025-01-03
- 黑龍江注射級DDM價格 2025-01-03
- 浙江二類械字號通氣鼻貼代理 2025-01-03
- 深圳提亮煥白乳液價格 2025-01-03
- 重慶獸藥殘留檢測儀技術指導 2025-01-03
- 成都中醫發光模型供應商 2025-01-03