遼寧個性化藥物安全性評價指標
新藥申請是申辦者采取的要求FDA考慮批準新藥在美國上市的正式步驟。在完成了Ⅲ期臨床試驗并獲得了藥物安全性評價信息后,申辦者提出新藥申請。現在,可以以電子方式提交臨床研究報告,CDISO正是基于這一要求而開發的用于數據提交/交換的標準。NDA的審評由藥理、化學、統計、醫學和藥物代謝等不同專業的人員組成的審核小組進行,并由消費者安全官統籌:(1)消費者安全官檢查所送資料是否完整。(2)審核小組審核。(3)召集**咨詢委員會會議,公開討論試驗的結果并提出委員會意見當NDA審核結束后,FDA將給申辦者一份核準信函并說明所需補充的資料或手續當所有手續齊全后,經FDA同意,寄發新藥上市許可核準書,作為藥物上市的法律依據。藥物安全性評價實驗哪家公司能做?遼寧個性化藥物安全性評價指標
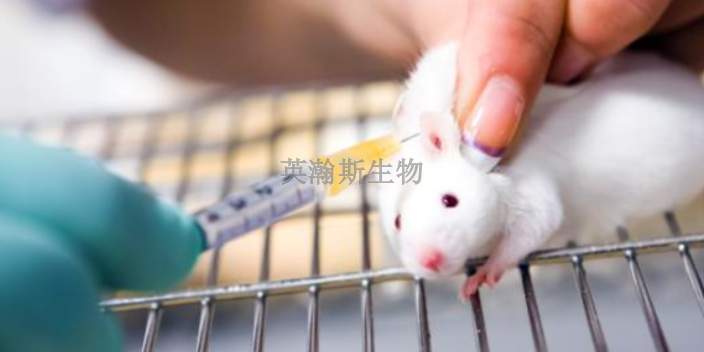
在獲得藥物安全性評價資料之后,藥物研究將進入臨床試驗階段。相對于在動物體內進行的臨床前研究,臨床試驗是指試驗對象是人體的硏究。根據研究目的和受試者的不同,人體臨床研究一般分為4期(-ⅣV期),I-Ⅲ期臨床研究的結果,連同臨床前期的數據提交給藥監評審機構,以獲得上市的批準。IV期臨床研究是新藥在批準上市后,進行相應的臨床研究,觀察在更大的范圍內使用這個新藥時,它的療效和不良反應、在特殊患者中的使用效果,以及是否要改進給藥劑量等。人體臨床研究的過程列于表2。浙江專注藥物安全性評價公司新藥從研制過渡到臨床,必須進行臨床前的藥物安全性毒理學評價。
監管科學研究旨在開發新的工具、標準和方法進行受監管藥物安全性評價。該學科是監管決策的基礎,是用于人用藥和獸藥整個生命周期中評估其質量、安全性和有效性的科學。在醫藥產品開發和評價中,所用的科學技術必須進行改進,在毒理學的現代化、推動臨床評價和個體化醫療的創新、創造新的方法以改進產品的生產工藝并提高產品質量、確保食品藥品監管機構已經為創新技術的評估做好充分準備、借助信息科學利用好各種數據、推行以預防為主的食品安全體系、加快制定醫療對策以抵御各種威脅和進一步發展社會和行為科學以幫助消費者在選擇產品時做出知情決策等8方面有重要作用。
藥物安全性評價的地位和價值體現在以下三個方面:1.在支持新藥臨床研究時,并不需要在進入臨床研究(I期)前完成所有相關研究,而是分階段來分別支持I、Ⅱ、Ⅲ期臨床研究,為如何進行臨床研究提供重要參考,具體體現在臨床研究方案中的給藥劑量(尤其是I期臨床研究的起始劑量)、安全性檢查/監測指標和檢測時機的確定,危險性的預測和救治措施的實施等方面;2.在臨床研究過程中,甚至上市后,出現非預期重要的安全性問題且難以判斷/預測其風險性等情況下,需再次進行有關的非臨床安全性研究(包括機制研究),通過臨床研究信息為非臨床安全性研究提供方向和目標,以減少臨床研究和(或)臨床應用的風險;3.在臨床研究完成后,受試藥的臨床有效性和安全性已有一個基本結論,此時藥物安全性評價的某些結果(如致*性等)可能是比較終確定受試藥是否批準上市(利弊權衡)的重要依據之一。藥物安全性評價,是指利用實驗動物進行的一系列實驗研究,主要觀察和測定藥物對機體的損害和影響。
FDA批準時已知的新型療法的特征包括藥物類別、***領域、優先審評、加速批準、孤兒藥狀態、接近監管期限批準和監管審查時間。從2001年到2010年,FDA批準了222種新型***藥物。生物制劑、精神類藥物、加速審批和接近監管期限的批準與更高的事件發生率呈***的統計學相關,突顯了在整個生命周期中對新型藥物安全性評價進行持續監測的必要性。這些研究針對美國FDA批準新藥上市后的安全性事件的主要研究結果和措施,為出于安全考慮而將藥品退市、上市后逐步增加的黑框警示以及FDA發布安全通訊提供依據。英瀚斯生物藥品安全性評價,專業藥品檢測實驗室。浙江專注藥物安全性評價公司
英瀚斯藥物安全性評價,為新藥候選化合物的確定及開發提供依據。遼寧個性化藥物安全性評價指標
為客觀評價藥物的安全性,應***理解實驗室檢查結果變化的統計學意義與臨床意義的關系,有統計學意義的檢查結果改變不一定有臨床意義,這要結合相關參數臨床上的參考值范圍和統計學意義產生的原因來綜合考慮;而沒有出現統計學意義并不一定意味著沒有臨床意義,應注意變化趨勢的明顯程度并結合所在實驗室參考值范圍等來綜合考慮,對個體結果進行定性分析并計算群體異常率,常常可以發現其變化的統計學和臨床意義。在此基礎上綜合判定與分析毒性與藥物的相關性。為此,建議結合下述因素進行綜合分析:①劑量效應關系;②與給藥前結果、同期對照組的比較;③受試動物歷史對照信息、流行病學的背景資料和動物飼養條件;④其他毒理學研究和評價的結果;⑤動物藥代/毒代動力學研究結果;⑥靶***毒性相關指標系統的綜合分析;⑦臟器組織病理學檢查及量化的結果。由此對毒性靶***、毒性反應及安全范圍進行綜合判斷。遼寧個性化藥物安全性評價指標
- 黑龍江哪家做病理實驗外包公司 2025-01-09
- 重慶生物病理實驗外包檢測 2025-01-09
- 浙江哪家做病理實驗外包服務 2025-01-09
- 河北個性化臨床前動物實驗研究 2025-01-08
- 寧夏靠譜的病理實驗外包服務 2025-01-08
- 福建靠譜的病理實驗外包檢測 2025-01-08
- 廣東哪家做病理實驗外包公司 2025-01-07
- 陜西生物病理實驗外包 2025-01-07
- 廣東個性化臨床前動物實驗哪家好 2025-01-07
- 云南專門做病理實驗外包哪家靠譜 2025-01-06
- 河北皮膚外用消毒涂藥器誰家的好 2025-01-09
- 遼寧口鏡頭口腔耗材公司 2025-01-09
- 湖北綠色環保洗鼻鹽怎么樣 2025-01-09
- 海安紅細胞生成素(EPO)檢測試劑盒(酶聯免疫吸附試驗法) 2025-01-09
- 陜西全腸道菌群檢測怎么樣 2025-01-09
- 浙江智能醫用純水節水設計 2025-01-09
- 清遠膠原蛋白肽廠商 2025-01-09
- 廣東奧索假肢廠家 2025-01-09
- CT掃描儀醫療設備維修團隊 2025-01-09
- 蘇州菊花茶 2025-01-09