河北個性化臨床前動物實驗研究
臨床前動物實驗的要求(1)從事藥物研究開發的機構的要求。應當具有與試驗研究項目相適應的人員、場地、設備、儀器和管理制度;所用試驗動物、試劑和原材料應當符合國家有關規定和要求;并應當保證所有試驗數據和資料的真實性。(2)研究用原料藥的規定。單獨申請注冊藥物制劑的,研究用原料藥必須具有藥品批準文號、《進口藥品注冊證》或者《醫藥產品注冊證》,該原料藥必須通過合法的途徑獲得。(3)境外藥物試驗研究資料的處理。藥品注冊申報資料中有境外藥物研究機構提供的藥物試驗研究資料的,必須附有境外藥物研究機構出具的其所提供資料的項目、頁碼的情況說明和證明該機構已在境外合法登記的經公證的證明文件,并經國家食品藥品監督管理局認可后,方可作為藥品注冊申請的申報資料。國家食品藥品監督管理局根據審查需要組織進行現場核查。生物藥臨床前動物實驗外包;河北個性化臨床前動物實驗研究
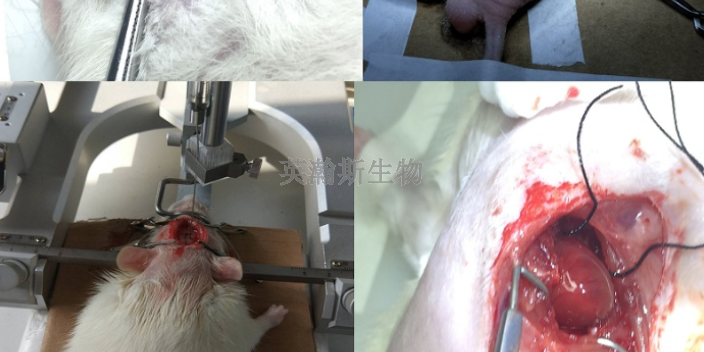
新藥往往需要臨床前動物實驗,從設計到上市通常需要10-15年的時間,經歷漫長的研發過程和層層考驗,同時需要大量的資本投入。藥物通過發現篩選、臨床前研究、臨床試驗、新藥NMPA/FDA上市申報等環節,比較終成為穩定、安全、有效的藥品,惠及人類健康。其中的每個研究階段都至關重要,特別是臨床前藥物研究獲得的結果對藥物進入臨床提供關鍵的數據指導,為優化臨床開發計劃提供有力的數據基礎。臨床前動物實驗是其中非常重要的一環,起到承上啟下的作用。河北個性化臨床前動物實驗研究英瀚斯專業做中成藥臨床前動物實驗外包。
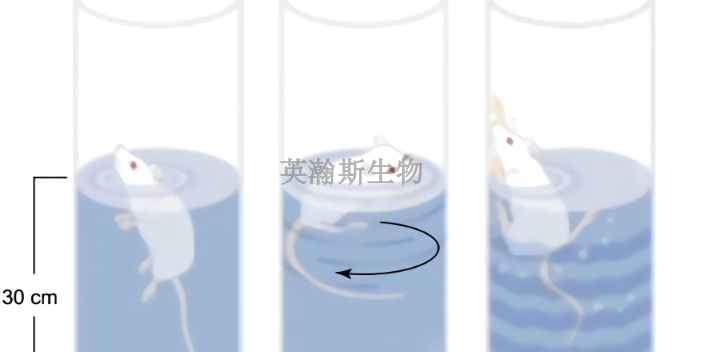
當臨床前動物實驗結果顯示化合物具有足夠的安全性并準備進入人體試驗時主辦者需要向FDA申請新藥臨床試驗investigationalNewDrugApplication,ND申請)。按照美國食品、藥品和化妝品法案(Food,DrugandCosmeticAct),此時的化合物已經成為研究藥物,將受到官方的監管。FDA收到藥物申報主辦者遞交的IND時,藥物申報主辦者,即負責藥物上市的公司硏究機構和其他組織,必須向FDA提供其對實驗動物所進行臨床前試驗的結果,以及進行人體試驗的具體計劃。在這個階段,FDA必須判斷藥物是否安全,是否達到實施人體試驗的標準。
預測人體反應:通過觀察動物對藥物的反應,科學家可以預測在人體中可能出現的情況,從而制定相應的應對策略。臨床前動物實驗通常遵循一定的步驟,包括選擇具有與目標疾病相似特征的動物模型、設計實驗方案、施用藥物并記錄相關信息等。這些實驗往往選用大鼠、小鼠或豬、狗、猴等大動物作為實驗對象,以確保實驗結果的可靠性和有效性。需要注意的是,臨床前動物實驗必須遵循嚴格的倫理和法律規定,確保動物的權益和福利得到保護。同時,實驗結果還需要經過充分的分析和總結,為后續的臨床試驗提供科學依據。總之,中成藥臨床前動物實驗是新藥研發過程中的關鍵環節,對于確保中成藥的安全性和有效性具有重要意義。中成藥臨床前動物實驗指標;

下面提供了關于臨床前動物實驗研究監測的具體建議:(1)術中監測:術中和術后對心率、心電圖、血壓和血氣的監測有助于獲得積極結果。(2)急性(短期)研究:建議**記錄生命體征,如手術時記錄的心律、呼吸頻率、脈搏和血壓。這些信息應與植入、放置或使用裝置、造影劑或其他裝置相關材料的時間相關聯,并在麻醉和手術記錄中注明。(3)慢性(長期)研究:慢性研究包括如下不同時期:①術后護理:建議遵循目前的實驗室實驗動物護理標準,保持動物體溫正常,盡量減少疼痛和***,并提供充足的液體和電解質。獲取動物生理信息的質量應與人類護理和康復中所獲得的信息相類似。此外,還應建立一個標準評估模式來控制壓力變量,以監測疼痛和體溫,并根據中期結果指導額外的保溫和止痛藥使用。化學藥臨床前動物實驗是什么?河北個性化臨床前動物實驗研究
化學藥臨床前動物實驗中心;河北個性化臨床前動物實驗研究
藥物在進入市場前必須通過一系列嚴格的試驗,其中包括化合物的合成、臨床前動物試驗和人體臨床試驗等。藥物試驗的不同階段將分別研究藥物的安全性、有效性、理想的給藥途徑、適宜的使用劑量,以及對患者生活質量的影響等。美國新藥評審系統被公認為在世界上是**嚴格的。根據Tufs藥物發展研究中心2001年的報告,平均起來,一種新藥從實驗室合成,篩選開始到***被批準上市,用于患者,共要花費大約8億美元,費時10-15年。在被篩選的5000-10000個化合物中,250個可以進入臨床前試驗,而其中只有5個可以進入臨床試驗,**終*有1個能被批準上市。河北個性化臨床前動物實驗研究
- 黑龍江哪家做病理實驗外包公司 2025-01-09
- 重慶生物病理實驗外包檢測 2025-01-09
- 浙江哪家做病理實驗外包服務 2025-01-09
- 河北個性化臨床前動物實驗研究 2025-01-08
- 寧夏靠譜的病理實驗外包服務 2025-01-08
- 福建靠譜的病理實驗外包檢測 2025-01-08
- 廣東哪家做病理實驗外包公司 2025-01-07
- 陜西生物病理實驗外包 2025-01-07
- 廣東個性化臨床前動物實驗哪家好 2025-01-07
- 云南專門做病理實驗外包哪家靠譜 2025-01-06
- 海安紅細胞生成素(EPO)檢測試劑盒(酶聯免疫吸附試驗法) 2025-01-09
- 陜西全腸道菌群檢測怎么樣 2025-01-09
- 浙江智能醫用純水節水設計 2025-01-09
- 廣東奧索假肢廠家 2025-01-09
- CT掃描儀醫療設備維修團隊 2025-01-09
- 廣西特膳有用嗎 2025-01-09
- 杭州蛋白分離離心管價位 2025-01-09
- 多抗進口需求 2025-01-09
- 金華清潤養生套裝報價 2025-01-09
- 陜西下肢器材機械外骨骼下肢器材 2025-01-09