西藏微流控脂質(zhì)體載藥
微流體法制備脂質(zhì)體是一種先進(jìn)的技術(shù),具有很多優(yōu)勢,如能夠精確控制脂質(zhì)體的尺寸、提高脂質(zhì)體的均勻性等。以下是微流體法制備脂質(zhì)體的關(guān)鍵技術(shù)參數(shù):一、流量比(FRR)流量比是微流體法制備脂質(zhì)體的一個關(guān)鍵參數(shù)。在多個研究中都表明了FRR對脂質(zhì)體的性能有著重要影響。例如,有研究指出,通過改變微流體通道中水相和乙醇相的流量比,可以調(diào)整脂質(zhì)體的尺寸和藥物負(fù)載量2427。當(dāng)FRR增加時,親水***物模擬裝載效率會增加,并且疏水***物模擬劑加載效率和FRR具有正線性相關(guān)性24。同時,F(xiàn)RR還能影響脂質(zhì)體的結(jié)構(gòu),通過改變FRR和初始脂質(zhì)濃度,可以控制脂質(zhì)體的單多層結(jié)構(gòu)27。此外,F(xiàn)RR也是影響脂質(zhì)體大小、蛋白質(zhì)載荷和釋放型材的關(guān)鍵因素20。脂質(zhì)體的結(jié)構(gòu)特點(diǎn)很多。西藏微流控脂質(zhì)體載藥
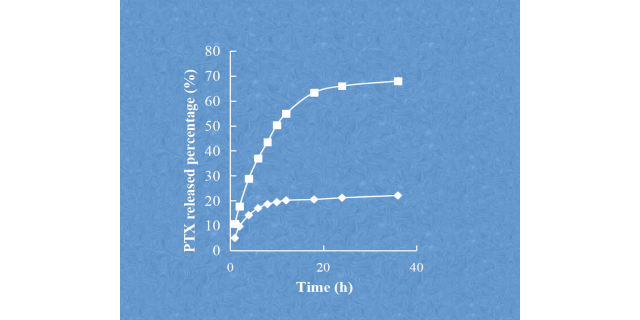
載藥脂質(zhì)體如何純化如果需要純化載藥脂質(zhì)體,通常會根據(jù)載藥脂質(zhì)體的性質(zhì)和所需純度要求選擇合適的純化方法。以下是一些可能的純化方法:1.超濾法:超濾可以用于去除較大的雜質(zhì)和未包埋的藥物。通過選擇適當(dāng)?shù)姆肿恿拷刂鼓ぃ瑢⑤d藥脂質(zhì)體溶液經(jīng)過超濾膜,較大的雜質(zhì)和未包埋的藥物將被截留,而較小的載藥脂質(zhì)體顆粒則通過膜孔。2.凝膠過濾法:凝膠過濾可以利用凝膠材料的孔隙大小分離分子。將載藥脂質(zhì)體溶液加入到凝膠柱中,通過洗脫的方式,較小的載藥脂質(zhì)體顆粒會通過凝膠柱,而較大的雜質(zhì)則會被截留在柱中。3.離心法:離心可以將載藥脂質(zhì)體顆粒沉淀到底部,去除上清液中的雜質(zhì)和未包埋的藥物。將載藥脂質(zhì)體溶液進(jìn)行高速離心,使載藥脂質(zhì)體顆粒沉淀到離心管底部,然后去除上清液中的雜質(zhì)和未包埋的藥物。4.柱層析法:柱層析可以利用吸附劑對溶液中分子的親和性分離。將載藥脂質(zhì)體溶液通過填充有吸附劑的柱子,通過洗脫的方式,使載藥脂質(zhì)體顆粒和雜質(zhì)分離出來。5.其他方法:根據(jù)具體情況,還可以考慮其他純化方法,如凝膠電泳法等。選擇合適的純化方法需要考慮載藥脂質(zhì)體的性質(zhì)、所需純度要求以及純化效率等因素。通常會結(jié)合多種方法進(jìn)行純化,以達(dá)到所需的純度和純凈度。吉林載藥脂質(zhì)體載藥主動藥物裝載?法,也稱為遠(yuǎn)程藥物裝載?法,涉及在空脂質(zhì)體產(chǎn)?后裝載藥物制劑。
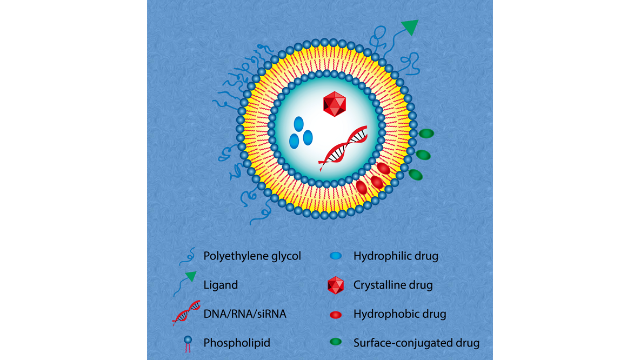
siRNA脂質(zhì)體
RNA干擾(RNAi)途徑允許siRNA和miRNAs負(fù)向調(diào)節(jié)蛋白表達(dá)。siRNA是21~23對核苷酸組成的雙鏈RNA,可誘導(dǎo)同源靶mRNA沉默。為了發(fā)揮作用,雙鏈siRNA分裂成兩個單鏈RNA:乘客鏈和引導(dǎo)鏈。乘客鏈被argonaute-2蛋白降解,而引導(dǎo)鏈則被納入RNAi誘導(dǎo)的沉默復(fù)合體中,該復(fù)合體結(jié)合與引導(dǎo)鏈互補(bǔ)的mRNA并將其切割。siRNA似乎具有***多種疾病的巨大潛力,因?yàn)樗鼈兛梢院苋菀椎叵抡{(diào)各種靶mRNA,而不考慮它們的位置(即在細(xì)胞核或細(xì)胞質(zhì)中),并且它們的特異性結(jié)合表明它們比傳統(tǒng)化學(xué)藥物誘導(dǎo)的副作用更少。作為一種新型的基于核酸的***策略,siRNA***與傳統(tǒng)的化學(xué)藥物相比具有許多優(yōu)勢。然而,為了促進(jìn)基于siRNA的***方法的發(fā)展,必須克服一些挑戰(zhàn),包括需要識別適當(dāng)?shù)陌谢蚝烷_發(fā)優(yōu)化的遞送系統(tǒng)。許多研究人員試圖利用陽離子脂質(zhì)體提高siRNA的細(xì)胞遞送和基因沉默效率。例如,由DC-6-14、DOPE和膽固醇組成的陽離子脂質(zhì)體被用于遞送螢火蟲熒光素酶特異性的siRNA。當(dāng)陽離子脂質(zhì)體與siRNA持續(xù)劇烈攪拌混合時,轉(zhuǎn)染效率提高,說明將siRNA加載到陽離子脂質(zhì)體上的方法可以調(diào)節(jié)轉(zhuǎn)染效率。siRNA脂叢的***應(yīng)用因靶蛋白而異。
microRNA脂質(zhì)體
microRNA是真核細(xì)胞中發(fā)現(xiàn)的短(約22mer)非編碼RNA,通過結(jié)合互補(bǔ)的mRNA序列發(fā)揮生物調(diào)節(jié)劑的作用。miRNA以初級miRNA的形式從其編碼的核基因轉(zhuǎn)錄,其長度為數(shù)百個核苷酸。RNaseIII酶,Drosha,將初級miRNA加工成pre-miRNA(長度為70個核苷酸),攜帶一個特征的發(fā)夾環(huán)。然后pre-miRNA移動到細(xì)胞質(zhì)中,在那里RNaseIII酶Dicer產(chǎn)生成熟的miRNA和乘客鏈。***,成熟的miRNA被整合到RNAi誘導(dǎo)的沉默復(fù)合體中,以降解它們的靶mRNA。由DOTMA、膽固醇和vitaminETPGS1k琥珀酸鹽組成的陽離子脂質(zhì)體被證明可以有效遞送pre-miRNA-133b,導(dǎo)致A549非小肺*細(xì)胞中成熟miRNA-133b的表達(dá)比對照組細(xì)胞增加2.3倍,Mcl-1蛋白的表達(dá)減少1.8倍。經(jīng)尾靜脈注射含有pre-miRNA-133b的陽離子脂質(zhì)體(1.5mg/kg)的ICR小鼠肺組織中成熟miRNA-133b的表達(dá)比接受含有紊亂的pre-mirna的陽離子脂質(zhì)體的小鼠高52倍。 脂質(zhì)體配方中各脂類的毒性的研究。
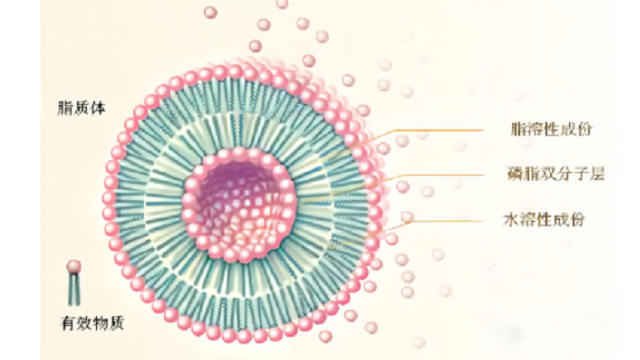
基因遞送用脂質(zhì)體隨著科學(xué)技術(shù)的進(jìn)步,與人類基因組及其在疾病***中的應(yīng)用相關(guān)的各種發(fā)現(xiàn)變得更加觸手可及。盡管有了這些發(fā)展,選擇一個合適的載體將基因傳遞到目標(biāo)是至關(guān)重要的。其中一種重要的載體是脂質(zhì)體,它可以將DNA、反義寡核苷酸、siRNA和其他潛在的藥物輸送到細(xì)胞核中。專門設(shè)計(jì)的脂質(zhì)體如陽離子脂質(zhì)體、pH敏感脂質(zhì)體、融合性脂質(zhì)體和基因體被用于基因遞送研究。由于DNA帶有強(qiáng)烈的負(fù)電荷,因此轉(zhuǎn)染細(xì)胞變得非常困難。DNA進(jìn)入細(xì)胞核可以用不同的方法進(jìn)行。它們大致可分為物理、化學(xué)、生物和機(jī)械。使用脂質(zhì)體傳遞DNA屬于化學(xué)范疇。陽離子脂質(zhì)體作為DNA轉(zhuǎn)染載體已顯示出良好的效果。然而,可以觀察到,轉(zhuǎn)染效果比較好的脂質(zhì)有三個主要成分:帶正電荷的頭基團(tuán)與帶負(fù)電荷的DNA相互作用,決定脂質(zhì)溶解度的連接基團(tuán)和有助于將脂質(zhì)錨定在雙分子層上的疏水性基團(tuán)。脂質(zhì)DNA絡(luò)合是由于脂質(zhì)表面的陽離子電荷使DNA靜電吸附而形成的。內(nèi)容物的遞送可能歸因于陽離子脂質(zhì)體的膜融合,同時避免了核仁和溶酶體對DNA的降解。脂質(zhì)體的大小是res***的重要決定因素。在這方面,當(dāng)脂質(zhì)體用于基因遞送時,內(nèi)皮細(xì)胞的通過是***道屏障。基因轉(zhuǎn)移**重要的靶***是肝臟。脂質(zhì)體根據(jù)室室結(jié)構(gòu)和層狀結(jié)構(gòu)可分為單層囊泡(ULVs)、寡層囊泡(OLVs)、多層囊泡(MLV)和多泡脂質(zhì)體(MVLs)。微流控脂質(zhì)體載藥惰性氣體
Arg-Gly-Asp (RGD)肽修飾的脂質(zhì)體增強(qiáng)核酸靶向整合素受體表達(dá)細(xì)胞傳遞的能力。西藏微流控脂質(zhì)體載藥
脂質(zhì)體靶向遞送中**核靶向功能已知**具有核靶向功能。為了增強(qiáng)質(zhì)粒DNA的核轉(zhuǎn)運(yùn),**與PAMAM樹狀大分子偶聯(lián),與DOPE(1:1)混合形成脂質(zhì)體。與聚亞胺相比,PAMAM-**/DOPE陽離子脂質(zhì)體增強(qiáng)了HEK293細(xì)胞中質(zhì)粒DNA的表達(dá),并顯示出較低的細(xì)胞毒性(m.w.25,000)。總的來說,靶向配體的修飾可以幫助實(shí)現(xiàn)特異性靶向,避免非特異性分布到肝臟和其他組織。然而,從商業(yè)化的角度來看,配體定制技術(shù)仍然面臨許多障礙,包括需要更流線型的制造工藝和改進(jìn)的質(zhì)量控制。西藏微流控脂質(zhì)體載藥
- 中國臺灣熒光染料luc 2025-01-17
- 江西熒光染料 2025-01-17
- 熒光染料Fluor 488 2025-01-17
- 熒光素鉀鹽熒光染料Cy3 2025-01-17
- 濟(jì)南熒光染料Fluor 647 2025-01-17
- 安徽細(xì)胞熒光染料 2025-01-17
- 中國香港武漢熒光染料 2025-01-17
- 西藏脂質(zhì)體載藥定做 2025-01-16
- 中國臺灣紅色熒光脂質(zhì)體載藥 2025-01-16
- 西藏微流控脂質(zhì)體載藥 2025-01-16
- 外泌體電鏡價格 2025-01-17
- 南京降血脂莫諾苯宗真實(shí)貨源 2025-01-17
- 安徽有什么矯形器行走器 2025-01-17
- 深圳高效細(xì)胞遷移檢測服務(wù)公司 2025-01-17
- 養(yǎng)心茶哪個牌子好 2025-01-17
- 寧波降血脂nmn貨源源頭 2025-01-17
- 浙江恒壓循環(huán)醫(yī)用純水機(jī)組供應(yīng)商 2025-01-17
- 浙江全自動醫(yī)用純水機(jī)組多少錢 2025-01-17
- 南京維修奧托博克假肢品牌 2025-01-17
- 四川女性低聚異麥芽糖婦科凝膠 2025-01-17