LncRNA-HMG在CRC化療耐藥中的關(guān)鍵作用
結(jié)直腸AI(CRC)是世界上較常見(jiàn)的惡性腫LIU之一。在化療或放療時(shí),會(huì)產(chǎn)生大量的活性氧來(lái)幫助殺死AI細(xì)胞。在化療耐藥的AI細(xì)胞中,清CHU ROS或脂質(zhì)過(guò)氧化物對(duì)于保護(hù)細(xì)胞免于鐵死亡和獲得耐藥性至關(guān)重要。因此,研究ROS平衡與腫LIU化療耐藥的協(xié)同機(jī)制將使我們對(duì)腫LIU治LIAO 有更好的認(rèn)識(shí)。

2024年9月,北京大學(xué)王崑及劉小鋒共同通訊在Redox Biol.(IF=10.7)上,發(fā)表“LncRNA-HMG incites colorectal cancer cells to chemoresistance via repressing p53-mediated ferroptosis”的研究成果。揭示LncRNA-HMG促進(jìn)結(jié)直腸AI化療耐藥機(jī)制,可能是結(jié)直腸AI的預(yù)后或治LIAO 靶點(diǎn)。
圖形摘要:
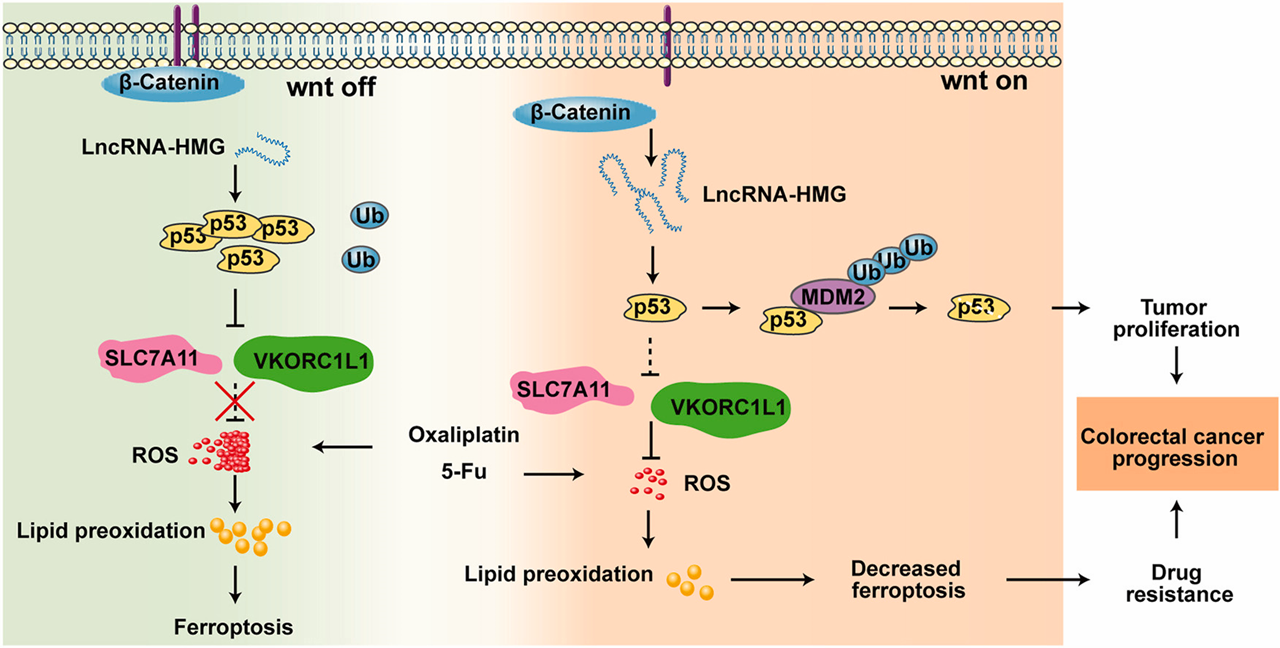
Highlights如下:
1)LncRNA-HMG與結(jié)直腸AI患者預(yù)后相關(guān)。
2)LncRNA-HMG抑制CRC細(xì)胞鐵死亡和化療耐藥
3)機(jī)制上,LncRNA-HMG與p53結(jié)合并促進(jìn)MDM2介導(dǎo)的p53降解,p53的降低誘導(dǎo)SLC7A11和VKORC1L1的上調(diào),消除過(guò)量的ROS,進(jìn)而促進(jìn)CRC細(xì)胞逃避鐵死亡并獲得化療耐藥性。
臨床相關(guān)性:
LncRNA-HMG在CRC組織中的高表達(dá)與結(jié)直腸AI患者預(yù)后不良相關(guān)。
功能研究:
敲減LncRNA-HMG,促進(jìn)CRC細(xì)胞鐵死亡和降低化療耐藥,而LncRNA-HMG過(guò)表達(dá)則相反。在體內(nèi),敲減LncRNA-HMG可減弱PDX腫LIU生長(zhǎng),促進(jìn)結(jié)直腸AI的化學(xué)敏感性。
機(jī)制研究:
(1)LncRNA-HMG減弱p53介導(dǎo)的鐵死亡
第一步,p53可能為L(zhǎng)ncRNA-HMG下游分子
為了探索LncRNA-HMG介導(dǎo)CRC細(xì)胞化療耐藥的分子機(jī)制。將TCGA結(jié)直腸AI數(shù)據(jù)分為L(zhǎng)ncRNA-HMG低組和LncRNA-HMG高組,差異基因富集分析發(fā)現(xiàn)p53信號(hào)明顯富集(圖1a-b)。STRING蛋白-蛋白互作分析表明p53是樞紐因子之一(圖1c)。綜上所述,LncRNA-HMG可能與p53結(jié)合,調(diào)控p53信號(hào)通路。
第二步,LncRNA-HMG調(diào)控p53及其下游靶點(diǎn)
研究表明p53作為一個(gè)關(guān)鍵的轉(zhuǎn)錄因子,通過(guò)抑制鐵凋亡抑制因子SLC7A11和VKORC1L1的表達(dá)來(lái)影響細(xì)胞內(nèi)ROS水平。WB檢測(cè)發(fā)現(xiàn),LncRNA-HMG敲減增加p53水平,降低SLC7A11和VKORC1L1水平;過(guò)表達(dá)LncRNA-HMG則相反(圖1d-e)。同樣,LncRNA-HMG缺失促進(jìn)5-Fu和奧沙利鉑治LIAO 后p53的升高,下調(diào)SLC7A11和VKORC1L1的表達(dá);過(guò)表達(dá)則相反(圖1f-g)。表明LncRNA-HMG調(diào)控p53及其下游靶點(diǎn)。
第三步,LncRNA-HMG降低p53的穩(wěn)定性,并減弱p53介導(dǎo)的ROS鐵死亡
根據(jù)報(bào)道,p53的蛋白穩(wěn)定性在控制p53水平中起重要作用。采用核糖體阻滯藥物環(huán)己亞胺(CHX)阻斷蛋白翻譯,進(jìn)一步分析p53的穩(wěn)定性。發(fā)現(xiàn),LncRNA-HMG過(guò)表達(dá),p53的穩(wěn)定性受到損害,而抑制LncRNA-HMG則增強(qiáng)了p53的穩(wěn)定性(圖1h-i)。顯示LncRNA-HMG降低了p53的穩(wěn)定性,并減弱了p53介導(dǎo)的ROS鐵死亡。
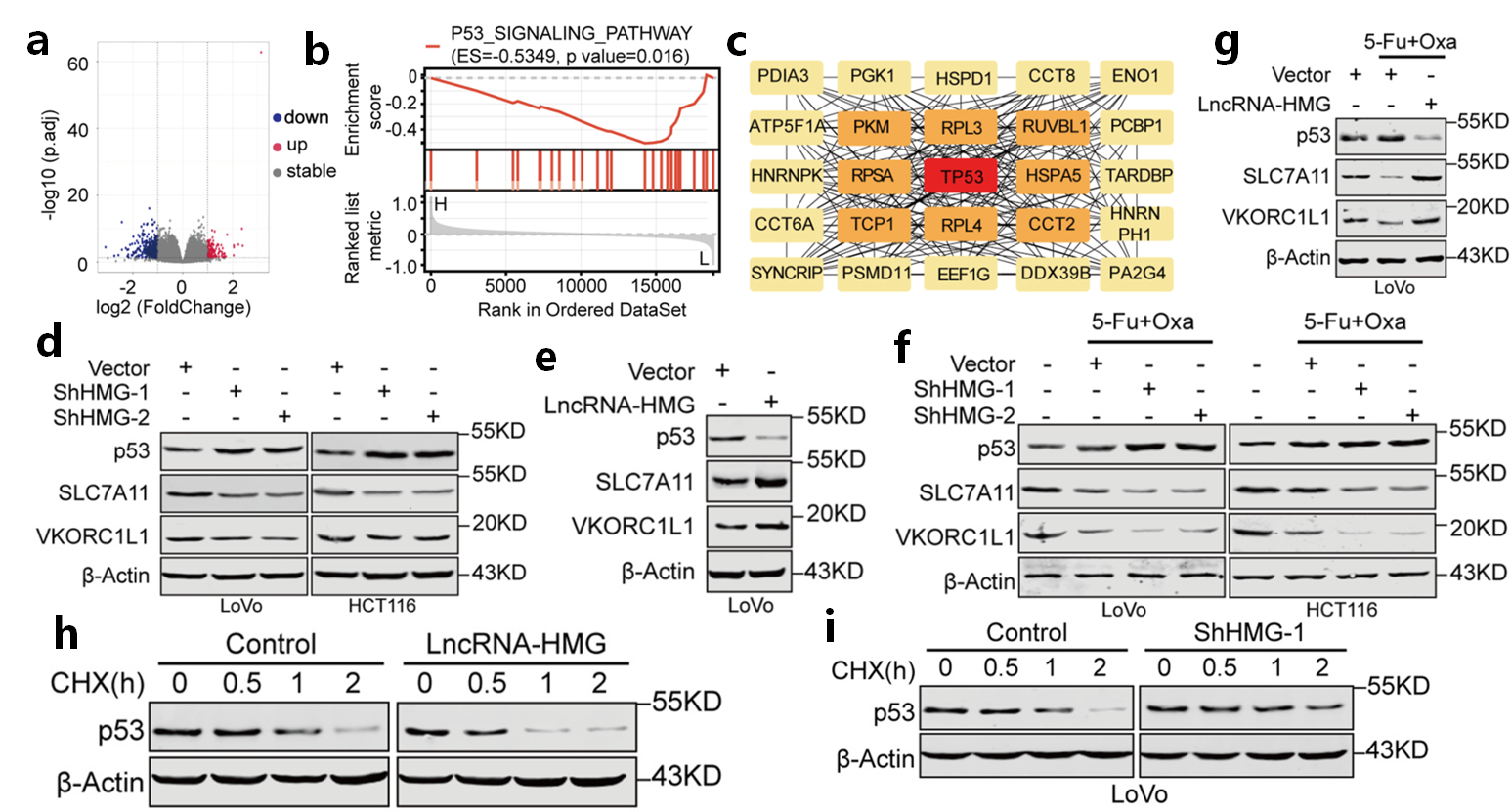
圖1 LncRNA-HMG減弱p53介導(dǎo)的鐵死亡(Ref. Fig 4)
(2)LncRNA-HMG協(xié)助MDM2增加p53的泛素化
第一步,LncRNA-HMG與p53互作,并促進(jìn)p53泛素化
為了研究LncRNA-HMG如何調(diào)節(jié)p53的穩(wěn)定性。RIP實(shí)驗(yàn)證實(shí)p53與LncRNA-HMG互作(圖2a)。泛素-蛋白酶體系統(tǒng)(UPS)對(duì)于調(diào)節(jié)p53的穩(wěn)定性至關(guān)重要。因此,利用蛋白酶體抑制劑MG132分析LncRNA-HMG調(diào)控p53穩(wěn)定是否依賴于UPS。發(fā)現(xiàn)MG132處理能逆轉(zhuǎn)LncRNA-HMG缺失誘導(dǎo)的p53升高(圖2b),表明LncRNA-HMG以蛋白酶體依賴的方式調(diào)節(jié)p53蛋白水平。此外,Co-IP分析顯示在LncRNA-HMG缺失的細(xì)胞中,p53的泛素化水平降低(圖2c),而LncRNA-HMG過(guò)表達(dá)可促進(jìn)p53的泛素化(圖2d)。表明LncRNA-HMG促進(jìn)p53泛素化,導(dǎo)致p53降解。
第二步,LncRNA-HMG增強(qiáng)MDM2對(duì)p53的活性
LncRNA-HMG如何促進(jìn)p53泛素化具有重要意義。MDM2是p53較重要的泛素連接酶。推測(cè)LncRNA-HMG可能增強(qiáng)了MDM2對(duì)p53的活性。Co-IP實(shí)驗(yàn)發(fā)現(xiàn),LncRNA-HMG同時(shí)結(jié)合p53和MDM2(圖2e)。RIP實(shí)驗(yàn)顯示,LncRNA-HMG與MDM2相互作用(圖2f)。RNA pulldown實(shí)驗(yàn)進(jìn)一步證實(shí)LncRNA-HMG與p53或MDM2結(jié)合(圖2g)。另外,LncRNA-HMG對(duì)MDM2水平?jīng)]有影響(圖2h)。LncRNA-HMG的缺失減少p53和MDM2之間的相互作用(圖2i),LncRNA-HMG過(guò)表達(dá)則增加MDM2介導(dǎo)的p53泛素化(圖2j)。此外,MDM2拮抗劑Nutlin-3消除了LncRNA-HMG對(duì)p53蛋白水平的影響(圖2k)。表明LncRNA-HMG促進(jìn)MDM2與p53的相互作用,增強(qiáng)p53的泛素化。后續(xù)的功能回復(fù)實(shí)驗(yàn)顯示,LncRNA-HMG依賴于p53調(diào)節(jié)ROS狀態(tài)(圖2l-m)。
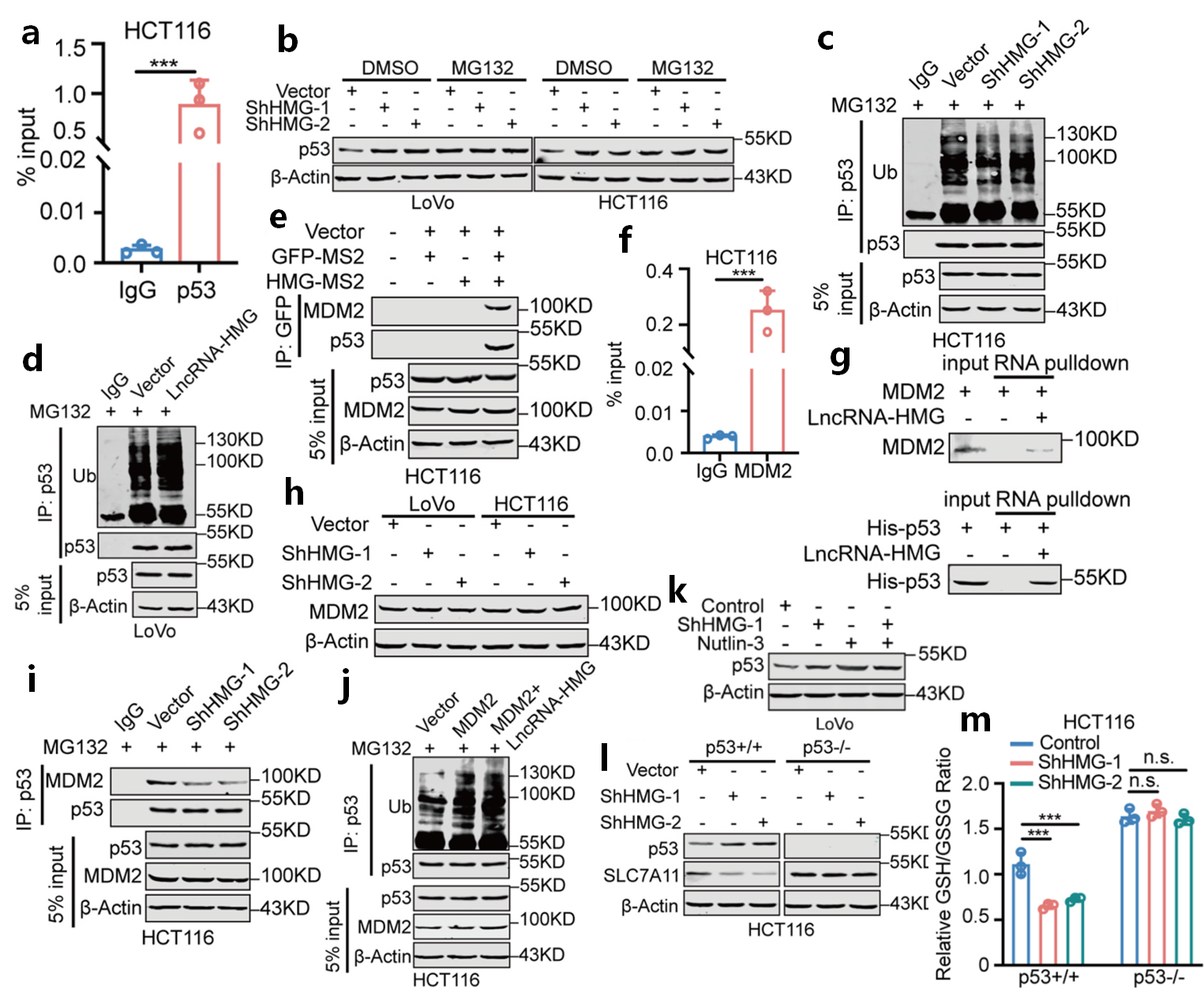
圖2 LncRNA-HMG協(xié)助MDM2增加p53的泛素化(Ref. Fig 5/S4)
(3)LncRNA-HMG是β-catenin的轉(zhuǎn)錄靶點(diǎn)
預(yù)測(cè)LncRNA-HMG啟動(dòng)子區(qū)結(jié)合的潛在轉(zhuǎn)錄因子(圖3a)。其中,Wnt/β-catenin信號(hào)在CRC進(jìn)展中的承擔(dān)重要角色。β-catenin過(guò)表達(dá)增加LncRNA-HMG的表達(dá)水平(圖3b),提示W(wǎng)nt/β-catenin調(diào)控LncRNA-HMG。結(jié)合β-catenin JI活劑LiCl和抑制劑iCRT14處理的結(jié)果,表明Wnt/β-catenin上調(diào)LncRNA-HMG的表達(dá)(圖3c-d)。
此外,分析顯示LncRNA-HMG啟動(dòng)子含有TCF結(jié)合元件(圖3e)。ChIP實(shí)驗(yàn)進(jìn)一步驗(yàn)證了這一點(diǎn)(圖3f)。同時(shí),含有LncRNA-HMG啟動(dòng)子區(qū)域的熒光素酶報(bào)告基因的轉(zhuǎn)錄活性被LiCl處理或β-catenin過(guò)表達(dá)明顯上調(diào),而iCRT14抑制了這種作用(圖3g)。表明LncRNA-HMG是β-catenin的下游轉(zhuǎn)錄靶點(diǎn)。
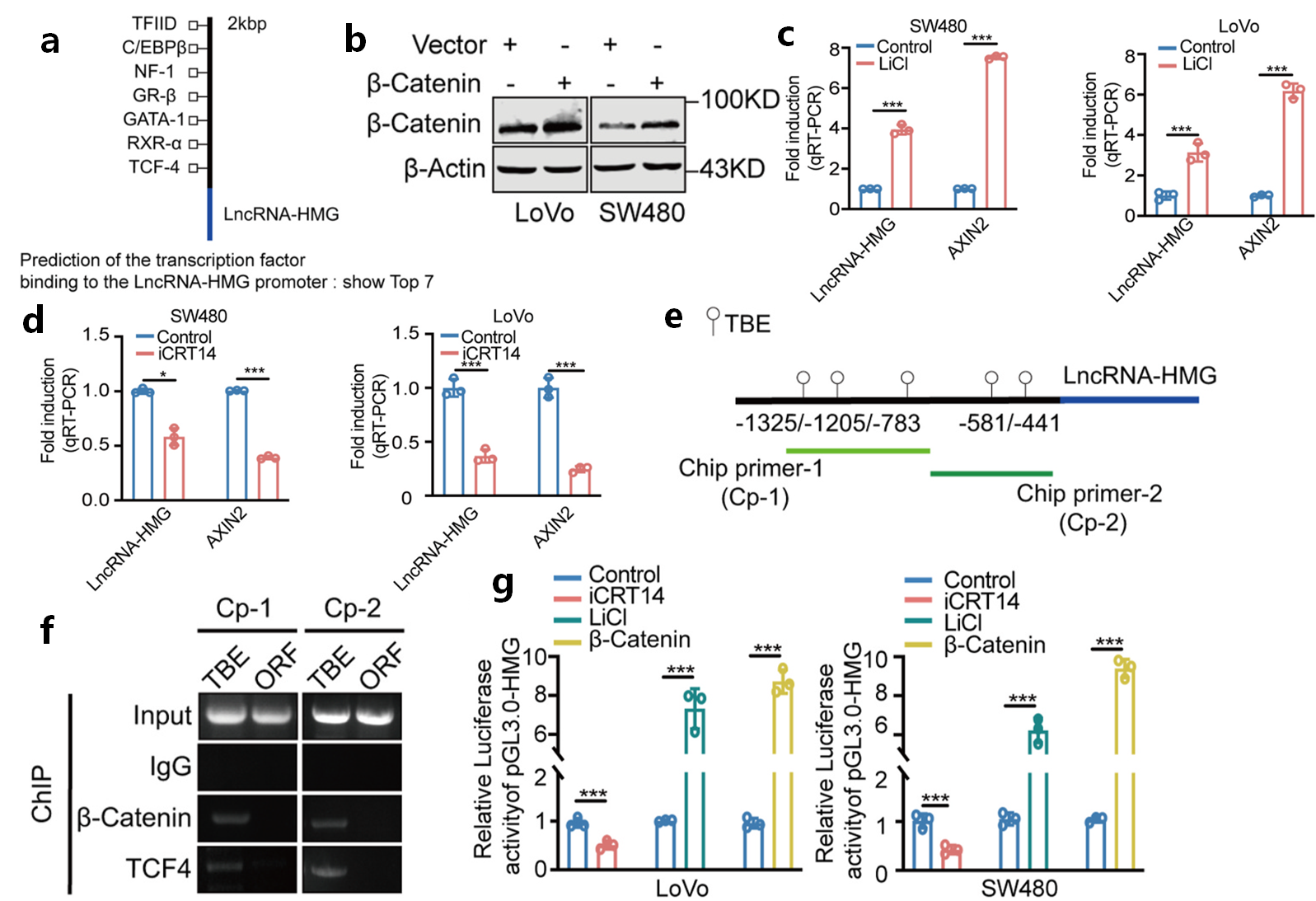
圖3 LncRNA-HMG是Wnt/β-catenin信號(hào)轉(zhuǎn)導(dǎo)的轉(zhuǎn)錄靶點(diǎn)(Ref. Fig 7)
結(jié)論:研究人員通過(guò)TCGA數(shù)據(jù)庫(kù)分析以篩選CRC中鐵死亡相關(guān)lncRNA。臨床上,LncRNA-HMG的異常高表達(dá)與CRC患者的預(yù)后較差相關(guān)。功能上,LncRNA-HMG保護(hù)CRC細(xì)胞在化療時(shí)免受鐵死亡,從而增強(qiáng)CRC細(xì)胞的耐藥性。機(jī)制上,LncRNA-HMG與p53結(jié)合并促進(jìn)MDM2介導(dǎo)的p53降解,隨后,p53的降低誘導(dǎo)SLC7A11和VKORC1L1的上調(diào),并消除過(guò)量的ROS,促進(jìn)CRC細(xì)胞從鐵死亡中逃脫并獲得化療耐藥性。此外,LncRNA-HMG也是β-catenin/TCF的下游轉(zhuǎn)錄靶標(biāo)。該研究突出了LncRNA-HMG在CRC化療耐藥中的關(guān)鍵作用,并暗示了其作為CRC治LIAO 靶點(diǎn)的潛在價(jià)值。
讓科學(xué)研究更簡(jiǎn)單,是我們的理念和追求!
背景:在臨床基礎(chǔ)科研過(guò)程中,都會(huì)遇到一個(gè)共同的挑戰(zhàn)——分子機(jī)制探索。
痛點(diǎn):做過(guò)機(jī)制研究的朋友,都要面臨一個(gè)共同的痛點(diǎn),即信號(hào)通路機(jī)制易做,分子互作機(jī)制太難,然而分子互作機(jī)制常常是高層次研究成果的重點(diǎn)部分。若不做,文章層次上不去;若做了,則海量的數(shù)據(jù)反復(fù)摸索,消耗大量精力,甚至無(wú)法上岸。
方案:針對(duì)這個(gè)痛點(diǎn),廣州基云生物重點(diǎn)推出“互作機(jī)制研究系統(tǒng)性解決方案”,包括免疫沉淀試驗(yàn)(IP、RIP、CHIP、CHIRP)和蛋白組芯片檢測(cè)試驗(yàn),協(xié)助輕松突破互作機(jī)制,讓科研成果更上一層樓。
推廣:十年蟄伏磨一劍,利劍出鞘,成人達(dá)己!我們團(tuán)隊(duì)期待與您進(jìn)行項(xiàng)目溝通、合作、共贏。
聯(lián)系方式:
咨詢熱線:400-7568-756

